مقاومت ضد میکروبی (AMR) مشکلی بزرگ و تهدیدی جدی برای سلامت عمومی محسوب می شود. کشورهایی که در آمد کم یا متوسط دارند بیشتر از سایر کشورها از نظر سلامت و اقتصاد، تحت تاثیر این مشکل قرار می گیرند. آنتی بیوتیک ها یکی از مهم ترین ابزار درمانی هستند اما بعد از توسعه فلوروکینولون ها در ابتدای دهه 1970 میلادی، هیچ کلاس آنتی بیوتیکی جدیدی وارد بازار نشده است. توقف در توسعه آنتی بیوتیک های جدید با خطر افزایش میکروارگانیسم های مقاوم به داروهای ضدمیکروبی همراه است.
اگر مقاومت میکروبی که تحت عنوان پاندمی خاموش هم شناخته می شود، کنترل نگردد می تواند تا چند دهه آینده سالیانه جان 10 میلیون نفر را در سراسر دنیا بگیرد.
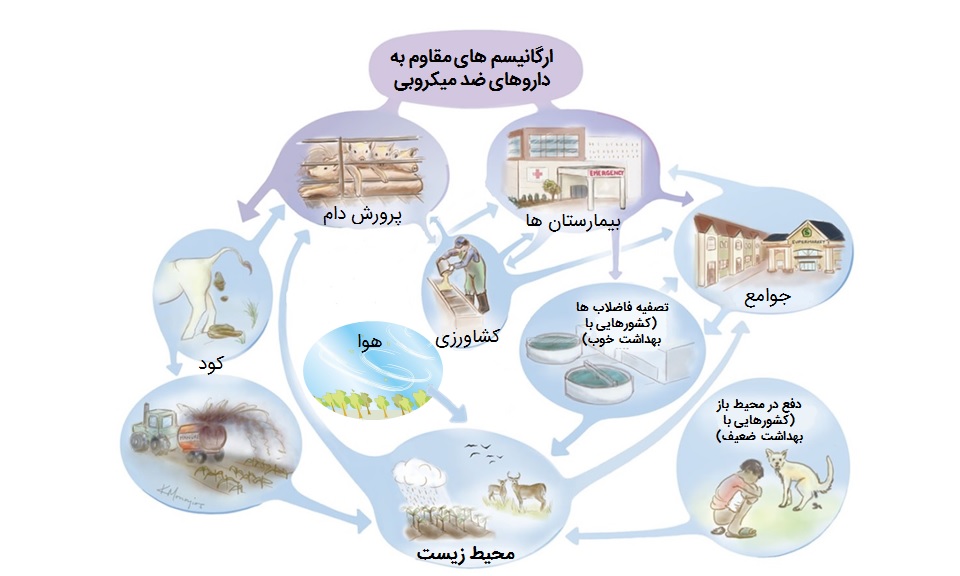
معمولا برای مقابله با مقاومت آنتی بیوتیکی، توجه ها بیشتر به سمت پزشکی، دامپزشکی و پرورش حیوانات تولید کننده غذا مثل دام، طیور و … است اما طی چند سال اخیر نقش و اهمیت محیط زیست نیز در توسعه و انتشار مقاومت ضدمیکروبی به خوبی شناخته شده است.
مقاومت آنتی بیوتیکی چگونه در محیط زیست اتفاق می افتد؟
مقاومت آنتی بیوتیکی می تواند به روش های مختلفی بین انسان ها، حیوانات و محیط زیست منتقل شود. آنتی بیوتیک ها از راه های متعددی مثل فاضلاب های شهری و بیمارستانی، مراکز پرورش دام، طیور و آبزیان، صنایع، پساب های کشاورزی حاوی کود حیوانی و شیرابه های زباله ها که حاوی آنتی بیوتیک هستند می توانند وارد محیط زیست شوند. نیمه عمر آنتی بیوتیک ها از چند ساعت تا چند صد روز متفاوت است اما در مجموع آنتی بیوتیک ها را جزو آلوده کننده های دائمی محیط زیست طبقه بندی می کنند.
افزایش استفاده از آنتی بیوتیک ها باعث ایجاد یک فشار انتخابی بر جمعیت های میکروبی که به طور طبیعی در محیط زیست وجود دارند، می شود. در حقیقت محیط زیست به عنوان مخزنی از قطعات ژنتیکی متحرک مختلف عمل کرده و می تواند ژن های مقاومت آنتی بیوتیکی را به گیاهان، انسان ها و حیوانات منتقل کند.
مانند سایر محصولات دارویی، آنتی بیوتیک های مصرف نشده یا تاریخ گذشته نیز همراه با زباله ها دور ریخته شده و نمی توانند تجزیه شوند؛ بنابراین وارد آب های زیر زمینی شده یا حین فرآیند تصفیه فاضلاب ها وارد آب های مخصوص پرورش آبزیان می شوند.
میکروارگانیسمهای محیطی که آنتی بیوتیک تولید می کنند، در مقایسه با میکروارگانیسم های بالینی، مقاومت ذاتی بیشتری نشان میدهند که به نظر میرسد کاملاً از فشار انتخابی متمایز است و با انتقال افقی ژن به دست نمیآید. خطر فزاینده انتقال مقاومت ذاتی میکروارگانیسمهای محیطی به پاتوژنهای انسانی در حال حاضر مشهود است و به یک نگرانی اصلی در مراکز مراقبتهای بهداشتی و درمانی تبدیل شده است.
مقاومت آنتیبیوتیکی ناشی از استفاده غیرمنطقی از آنتیبیوتیکها و افزایش فراوانی باکتریهای مقاوم و مکانیسمهای مقاومت در محیط، امروزه به عنوان «آلودگی مقاومت آنتیبیوتیکی» نامیده شده و در اصل نوعی آلودگی در نظر گرفته می شود.
فضولات و مواد دفعی
فضولات و مواد دفعی فراوانی که توسط انسان ها و حیوانات در سراسر دنیا تولید می شوند، به طور گسترده ای جمعیت های میکروبی محیط را تحت تاثیر قرار می دهند. انسان ها و حیوانات اهلی حدود 96 تا 98% زیست توده (biomass) پستانداران خشکی زی را تشکیل می دهند. تخمین زده می شود که دفعیات چنین جمعیت عظیمی از سال 2003 تا کنون بیش از 52 میلیارد کیلوگرم در سال افزایش یافته است و انتظار میرود که کل مدفوع تولید شده تا سال 2030 به حداقل 4.6 تریلیون کیلوگرم در سال برسد. مواد دفعی حیوانات تولید کننده غذا به خصوص طیور، گاو و گوسفند حدود 4 برابر انسان است که اهمیت مدیریت صحیح فضولات در مراکز پرورش دام و طیور را نشان می دهد زیرا این مواد می توانند حاوی باکتری های مقاوم (ARBs) یا ژن های مقاومت (ARGs) باشند. اگرچه اکثر کشورهای توسعه یافته تصفیه فاضلاب موثری برای پسماندهای انسانی دارند، اما 73 درصد نقاط جهان هیچ تصفیه مناسبی برای پسماندها ندارند. وضعیت مدیریت پسماند برای حیوانات اهلی حتی بدتر و به معنی مقادیر زیاد فضولات و مواد دفعی تصفیه نشده است که وارد محیط زیست شده و آب و غذا را آلوده و سلامت عمومی را تهدید می کنند. بنابراین بهبود وضعیت بهداشت و تصفیه پسماندها برای کاهش AMR ضروری است.
فاضلاب ها
فاضلاب ها یکی از راه های مهم در انتشار ارگانیسم های مقاوم به آنتی بیوتیک محسوب می شوند. اگرچه تصفیه ثانویه و ثالثیه فاضلاب به طور قابل توجهی بار میکروبی، به خصوص باکتری های مقاوم به آنتی بیوتیک، را 10 تا 1000 برابر کاهش می دهد، اما همه باکتری های مقاوم را از بین نمی برد. سرنوشت باکتری های مقاوم و خطر آنها به دلیل رها شدن در محیط زیست به شدت به نوع و میزان تصفیه فاضلاب بستگی دارد. اگرچه، صرف نظر از تصفیه، اغلب باکتری های مقاوم موجود در پساب ها وارد آب های سطحی شده و سلامت مصرف کنندگان این منابع آبی را به خطر می اندازند. هم چنین در مناطقی که از فاضلاب ها یا پساب های تصفیه شده برای آبیاری محصولات کشاورزی استفاده می شود (که امری رایج در سراسر دنیا می باشد) باکتری ها از جمله باکتری های مقاوم می توانند باعث آلودگی گیاهان و سبزیجات برگدار مورد مصرف انسان ها و حیوانات شوند. به علاوه آبیاری با فاضلاب ها سبب آلودگی آب های سطحی نیز می شود و از این طریق کیفیت آب را تحت تاثیر قرار می دهد. با این که انتشار باکتری های مقاوم و ژن های مقاومت از طریق فاضلاب ها به خوبی شناخته شده است، اطلاعات کمی در مورد اهمیت آن در توسعه مقاومت آنتی بیوتیکی وجود دارد. یکی از علل این موضوع این است که تشخیص منشا یک باکتری خاص در فاضلاب دشوار می باشد. بر اساس تحقیقات انجام شده، بیمارستان ها و صنعت کشاورزی دو منبع مهم برای ورود باکتری های مقاوم یا ژن های مقاومت به فاضلاب ها می باشند.
خاک
اجزای مورد نیاز برای سلامت خاک شامل مواد آلی و میکروب ها از جمله باکتری و قارچ است. ترکیبات آلی در حقیقت غذای این میکروب ها هستند، ساختار خاک را پایدار کرده و سبب افزایش باروری آن می شوند. در کشاورزی معمولا از کود به عنوان یک منبع اضافی برای مواد آلی استفاده می شود. با این حال کودها حاوی میکروب ها از جمله باکتری های مقاوم به آنتی بیوتیک هستند. لوله گوارش حیوانات اهلی شامل بسیاری از پاتوژن های زئونوز و همسفره (commensal) است که به مقدار زیادی همراه با مدفوع دفع می شوند. بنابراین کودی که به خوبی آماده و پردازش نشده باشد می تواند حاوی پاتوژن های مقاوم به آنتی بیوتیک باشد و باعث آلودگی خاک، آب و غذا می شوند. هم چنین خاک مانند منابع آبی توسط پسماندهای بیمارستانی، تصفیه خانه ها، پرورش آبزیان و … نیز آلوده می گردد. برخی از آنتی بیوتیک ها با خاک پیوند شیمیایی تشکیل داده و در آن پایدار باقی می مانند. هم چنین فاکتورهایی مانند بافت خاک و پایداری ژن های مقاومت آنتی بیوتیکی نقش مهمی در مدت زمان باقی ماندن مقاومت آنتی بیوتیکی در خاک دارند. هم چنین آلودگی خاک با فلزات سنگین و زیست کش ها (biocides) نیز امری محتمل است و می تواند در ایجاد مقاومت آنتی بیوتیکی در باکتری های موجود در خاک نقش داشته باشد.
فلزات سنگین
مقاومت نسبت به آنتی بیوتیک ها و فلزات شباهت های ساختاری و عملکردی زیادی با یکدیگر دارند. همانند مقاومت به آنتی بیوتیک ها، مقاومت به فلزاتی نظیر آرسنیک، روی، کبالت، منگنز و نقره نیز از طریق مکانیسم های زیر اتفاق می افتد:
- کاهش نفوذ پذیری غشا مانند مقاومت به بتالاکتام ها، سیپروفلوکساسین، تتراسایکلین و کلرامفنیکل
- تغییر فلز مانند مقاومت به کلرامفنیکل و بتالاکتام ها
- بیرون کردن فلزات از قبیل روی، نیکل، مس، کبالت و کادمیوم همانند مقاومت به کلرامفنیکل، تتراسایکلین و بتالاکتام ها
- تغییر نقطه هدف روی، مس و جیوه
- اتصال یا محدود کردن یون های فلزی به گونه ای که از سایر اجزای سیستم بیولوژیکی جدا شوند (metal sequestration) برای فلزاتی مثل مس، کادمیوم و روی
اطلاعات زیادی مبنی بر سمیت و قابلیت جا به جایی فلزات در اکوسیستم های آبی و خاکی وجود دارد. ترکیب آنتی بیوتیک ها، فلزات و زیست کش ها در خاک از حداقل غلظت مورد نیاز برای ایجاد مقاومت آنتی بیوتیکی بیشتر می شود. از طرفی باکتری هایی که حامل ژن های مقاومت به فلزات هستند (این ژن ها بیشتر روی پلاسمید قرار دارند)، در مقایسه با آنهایی که این ژن ها را ندارند، بیشتر ژن های مقاومت آنتی بیوتیکی را حمل و منتشر می کنند.
زیست کش ها
محصولات زیست کش حاوی ترکیبات شیمیایی هستند که خاصیت میکروبیواستاتی یا میکروبیوسید (میکروب کشی) دارند و علیه طیف وسیعی از میکروارگانیسم ها موثر می باشند. ضدعفونی کننده ها یا زیست کش ها به وفور در صنایع، بیمارستان ها، پاک کننده ها و … استفاده می شوند. در اروپا بازاریابی، مصرف و دفع و از بین بردن زیست کش ها تحت قوانین و شرایط خاصی انجام می شود. این قوانین استفاده از زیست کش ها در دامپزشکی را هم کنترل می کنند. رایج ترین ضدعفونی کننده ها شامل فرمالدهید، کلرهگزیدین و ترکیبات چهارتایی آمونیوم می باشند. استفاده از این ترکیبات با دوزی کمتر از دوز مهارکننده منجر به جهش در میکروب ها و مقاومت ضدمیکروبی می شود. ژن های مقاومت به زیست کش ها اغلب روی پلاسمیدها قرار می گیرند. وجود همزمان ژن های مقاومت به زیست کش ها و مقاومت آنتی بیوتیکی بر روی ژنوم خارج کروموزومی باعث تقویت انتقال آنها بین پاتوژن ها یا جمعیت های میکروبی می شود. برای مثال مقاومت همزمان به زیست کش بنزالکونیوم کلراید و آنتی بیوتیک ها منجر به 8 برابر شدن مقاومت استافیلوکوکوس اورئوس به آنتی بیوتیک ها می شود.
هوا
با اینکه غیر محتمل به نظر می رسد اما مقاومت آنتی بیوتیکی و ژن های مقاومت، به خصوص در کشورهای صنعتی، در هوا هم وجود دارند. ژن های مقاومت آنتی بیوتیکی موجود در هوا می توانند منجر به مقاومت نسبت به آنتی بیوتیک های مهم درمانی مثل ونکومایسین شوند. در نتیجه تنفس هوای شهرها به دلیل داشتن ژن های مقاومت آنتی بیوتیکی می تواند برای سلامتی خطرناک باشد. هم چنین مشاهده باکتری های مقاوم و ژن های مقاومت در دستگاه تنفس فوقانی، نقش هوا در انتشار مقاومت آنتی بیوتیکی را نشان می دهد. هم چنین برخلاف باکتری های مقاوم و ژن های مقاومت موجود در خاک، این ترکیبات در آب و هوا به شدت متحرک هستند و انتشار آنها راحت تر صورت می گیرد.
نتیجه گیری
در نهایت می توان نتیجه گرفت که محیط زیست به عنوان یک مخزن برای باکتری های مقاوم و ژن های مقاومت عمل کرده و به توسعه مقاومت ضد میکروبی کمک می کند. از جمله رایج ترین راه های انتقال باکتری های مقاوم به محیط زیست می توان به فضولات و مواد دفعی، فاضلاب ها و استفاده از کودهای حیوانی اشاره کرد. علاوه بر آنها بر اساس مطالعات جدید، هوا هم در انتقال مقاومت آنتی بیوتیکی نقش داشته و حتی ترکیباتی مثل فلزات سنگین یا زیست کش ها هم می توانند در توسعه مقاومت آنتی بیوتیکی نقش داشته باشند. بنابراین باید مدیریت و ارزیابی خطر در محیط زیست هم به منظور کاهش مقاومت آنتی بیوتیکی صورت پذیرد و به نقش و اهمیت محیط زیست در توسعه مقاومت آنتی بیوتیکی توجه شود.