مقاومت ضدمیکروبی (AMR)
داروهای ضد میکروبی مثل آنتیبیوتیکها، داروهای ضدویروس، ضدقارچ و ضدانگل، برای جلوگیری و درمان عفونتها در انسان، حیوان و گیاه استفاده میشوند. مقاومت ضد میکروبی (Antimicrobial Resistance) زمانی اتفاق میافتد که میکروبها دیگر به این داروها جواب نمیدهند. در نتیجه، درمان عفونت سختتر یا حتی غیرممکن میشود و خطر پخش شدن بیماری، بدحال شدن افراد، ناتوانی و مرگ افزایش پیدا میکند.
این مقاومت بهطور طبیعی و در طول زمان به دلیل تغییرات ژنتیکی در میکروبها ایجاد میشود، اما استفاده نادرست و زیاد از داروهای ضد میکروبی در پزشکی، دامپزشکی و کشاورزی باعث میشود این مقاومت خیلی سریعتر گسترش پیدا کند.
اهمیت مقاومت ضدمیکروبی
داروهای ضد میکروبی پایه و اساس بسیاری از درمانهای پزشکی هستند. اگر این داروها بیاثر شوند، درمان عفونتهای معمول و انجام عملهای مهم مثل شیمیدرمانی، سزارین یا پیوند اعضا بسیار سخت میشود. عفونتهای مقاوم همچنین روی سلامت حیوانات و گیاهان اثر میگذارند، باعث کاهش تولید در مزارع شده و امنیت غذایی را تهدید میکنند. AMR هزینههای زیادی به سیستمهای درمانی و اقتصاد کشورها تحمیل میکند، مثل نیاز به درمانهای گرانتر، بستری طولانیتر بیماران و کاهش بهرهوری در بخش کشاورزی.
این مشکل همه کشورها، چه فقیر و چه ثروتمند را تحت تأثیر قرار میدهد. کمبود آب و بهداشت مناسب، کنترل ضعیف عفونت در خانهها، بیمارستانها و مزارع، دسترسی محدود به واکسنها و داروهای باکیفیت، ناآگاهی مردم و رعایت نشدن قوانین مربوط به مصرف دارو، همگی باعث گسترش AMR میشوند. مردم مناطق کمدرآمد و گروههای آسیبپذیر بیشترین آسیب را از این مشکل میبینند.

روشهای اصلی تشخیص مقاومت در اروپا
در اروپا، آزمایشگاهها عمدتاً از استانداردهای EUCAST (European Committee on Antimicrobial Susceptibility Testing) پیروی میکنند. این کمیته معیارهای دقیق و بهروزی برای انجام آزمایشهای حساسیت دارویی و تفسیر نتایج ارائه میدهد. مهمترین روشهای مورد استفاده عبارتاند از:
۱. روش انتشار دیسک (Disk Diffusion Method)
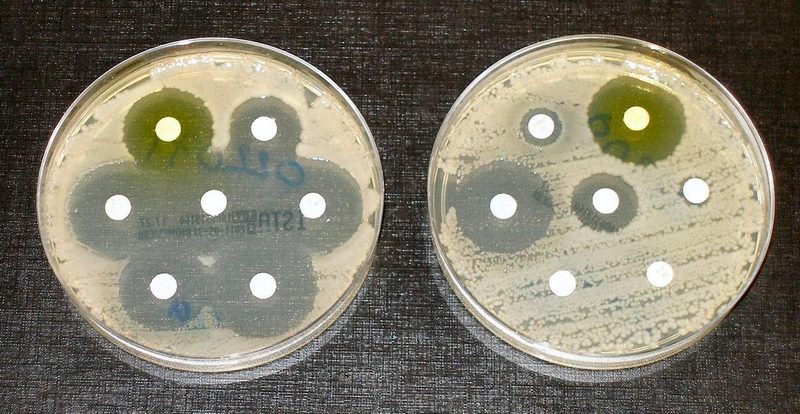
این روش ساده و پرکاربرد در بیشتر آزمایشگاهها اجرا میشود. در این روش، باکتری روی سطح محیط کشت آگار پخش شده و دیسکهای حاوی آنتیبیوتیک روی آن قرار میگیرند. پس از انکوباسیون، هالهای شفاف از عدم رشد باکتری در اطراف دیسک دیده میشود. قطر این هاله با جداول EUCAST مقایسه شده و نتیجه به صورت یکی از سه حالت زیر گزارش میشود:
- S (Susceptible): باکتری نسبت به آنتیبیوتیک حساس است.
- I (Susceptible, Increased exposure): دارو مؤثر است، اما باید با دوز بالاتر یا روش مصرف خاص استفاده شود.
- R (Resistant): باکتری در برابر دارو مقاوم است.
این روش به دلیل سادگی و هزینه پایین، هنوز پرکاربردترین شیوه در آزمایشگاههای میکروبشناسی است.
۲. تعیین حداقل غلظت مهارکننده (MIC)
روش MIC (Minimum Inhibitory Concentration) میزان کمترین غلظت آنتیبیوتیکی را تعیین میکند که میتواند رشد باکتری را متوقف کند. این مقدار معمولاً بر حسب میلیگرم بر لیتر (mg/L) گزارش میشود.
روشهای تعیین MIC شامل موارد زیر است:
- Microdilution broth method روش مرجع (Reference method) که در آن رقتهای مختلف آنتیبیوتیک در محیط مایع آزمایش میشوند.
- E-test (نوار گرادیانی)روشی سریع و ساده که مقدار MIC را روی نوار مشخص میکند.
- سیستمهای خودکار (Automated systems) دستگاههایی مانند VITEK 2, BD Phoenix, و MicroScan WalkAway که به طور خودکار رشد باکتریها و MIC را اندازه میگیرند.
نتایج MIC نیز بر اساس جداول EUCAST به صورت S، I یا R تفسیر میشوند.

روشهای مولکولی در تشخیص مقاومت
علاوه بر روشهای فنوتیپی (ظاهری)، امروزه روشهای مولکولی (Genotypic methods) برای شناسایی مستقیم ژنهای مقاومت بسیار پرکاربرد شدهاند. این روشها دقت بالایی دارند و برای شناسایی سریع سویههای چندمقاومتی به کار میروند.
روشهای مختلفی برای شناسایی مقاومت باکتریها در برابر عوامل ضد میکروبی در آزمایشگاهها به کار میرود. این روشها شامل روشهای فنوتیپی (ویژگیهای ظاهری و قابل مشاهده باکتری) و روشهای ژنوتیپی (ویژگیهای ژنتیکی باکتری) هستند.
روشهای فنوتیپی (Phenotypic methods)
۱. انتشار دیسک (Disk diffusion)
روش انتشار دیسک دیگر در پایش AMR در حیوانات و مواد غذایی مورد استفاده قرار نمیگیرد، اما هنوز هم بهطور روتین در آزمایشگاههای میکروبیولوژی بالینی کاربرد دارد.
در این روش، یک محیط آگار با سوسپانسیون باکتری تلقیح میشود و سپس دیسکهای کاغذی حاوی عوامل ضد میکروبی روی آن قرار داده میشوند.
پس از انکوباسیون، اگر عامل ضد میکروبی رشد باکتری را مهار کند، یک ناحیه شفاف اطراف دیسک ایجاد میشود که به آن منطقه مهار گفته میشود.
قطر این ناحیه مهار نشان میدهد که آیا باکتری نسبت به آن ماده حساس (ناحیه بزرگتر) یا مقاوم (ناحیه کوچکتر یا فاقد ناحیه) است.
EUCAST یک روش استاندارد انتشار دیسک را توسعه داده است که با نقاط برش حداقل غلظت مهارکننده (MIC breakpoints) هماهنگ در سطح اروپا تنظیم شده است.
۲. رقیقسازی در محیط مایع و آزمون حداقل غلظت مهارکننده (Broth microdilution & MIC tests))
در روش رقیقسازی در محیط مایع (broth microdilution)، چاهکهای کوچکی با محیط مایع (broth) که حاوی غلظتهای متفاوتی از یک عامل ضد میکروبی هستند پر میشوند. سپس باکتریها به این چاهکها افزوده میشوند و در شرایط مناسب انکوبه میگردند تا رشد کنند.
رشد باکتریها باعث ایجاد کدری در محیط یا تشکیل رسوبی از سلولها در ته چاهک میشود.
نتیجه آزمون بر اساس کمترین غلظت عامل ضد میکروبی که رشد قابل مشاهده باکتری را مهار میکند ثبت میشود. این مقدار را حداقل غلظت مهارکننده (MIC) مینامند که معمولاً با واحد میلیگرم بر لیتر (mg/L) یا میکروگرم بر میلیلیتر (µg/mL) بیان میشود.
روشهای ژنوتیپی (Genotypic methods)
توالییابی کامل ژنوم (Whole Genome Sequencing – WGS
توالییابی کامل ژنوم (WGS) یک روش تایپ مولکولی است که برای شناسایی ژنهای خاص مقاومت ضد میکروبی (AMR genes) در ژنوم باکتری به کار میرود.
در این روش، تقریباً کل توالی DNA باکتری تعیین میشود و سپس با یک پایگاه داده شامل توالی ژنهای شناختهشده مقاومت مقایسه میگردد تا وجود این ژنها در ژنوم شناسایی شود.
اگرچه WGS وضوح بسیار بالایی از ویژگیهای ژنتیکی باکتریها ارائه میدهد، اما باید توجه داشت که وجود یک ژن به تنهایی نمیتواند پیشبینی دقیقی از بروز واقعی مقاومت در عمل باشد، زیرا ممکن است ژن حضور داشته باشد ولی بیان (expression) نشود و باکتری در واقع مقاومت فنوتیپی واقعی نداشته باشد.
تفسیر مقاومت ضد میکروبی (Interpreting Antimicrobial Resistance)
تفسیر نتایج آزمون حساسیت ضد میکروبی (AST) بر اساس استانداردهای موجودی انجام میشود که توسط دو نهاد اصلی تدوین شدهاند:
- EUCAST (کمیته اروپایی آزمون حساسیت ضد میکروبی مستقر در اروپا)
- CLSI (مؤسسه استانداردهای بالینی و آزمایشگاهی مستقر در ایالات متحده آمریکا)
نتایج AST بر اساس دو شاخص اصلی تفسیر میشوند:
- نقاط برش بالینی (Clinical Breakpoints – CBPs)
- مقادیر حد آستانه اپیدمیولوژیک (Epidemiological Cut-off Values – ECOFFs)
این طبقهبندیها توسط پزشک یا دامپزشک برای انتخاب مؤثرترین عامل ضد میکروبی به کار میرود.
مقادیر حد آستانه اپیدمیولوژیک (Epidemiological Cut-off Values – ECOFFs)
مقادیر ECOFF برای تقسیم میکروارگانیسمها به دو گروه به کار میرود:
- تیپ وحشی (Wild Type) – فاقد مکانیسم مقاومت اکتسابی
- غیر تیپ وحشی (Non-Wild Type) – دارای مکانیسم مقاومت اکتسابی
استفاده از ECOFF اهمیت دارد زیرا تغییرات جزئی در حساسیت باکتریها ممکن است نشاندهنده ظهور مقاومت جدید باشد و این اطلاعات برای تحقیقات هدفمندتر یا اقدامات کنترلی مناسب مفید هستند.
زمانی که باکتری از طریق یک مکانیسم مشخص و کارآمد مقاومت را بهدست میآورد، نتایج MIC معمولاً دو زیرجمعیت اصلی را نشان میدهد:
- یکی کاملاً حساس (susceptible)
- دیگری کاملاً مقاوم (resistant)
مقدار ECOFF نشاندهندهی مقدار MIC یا قطر ناحیه مهار است که در بالاتر از آن، کاهش قابل تشخیص در حساسیت پاتوژن مشاهده میشود.
مقایسه CBP و ECOFF
- CBP برای تعیین اثربخشی درمانی بالینی داروی ضد میکروبی طراحی شده است و ممکن است نتواند مقاومتهای نوظهور را تشخیص دهد.
- در مقابل، ECOFF هر گونه انحراف از جمعیت حساس طبیعی (wild type) را شناسایی میکند، حتی اگر این تغییر هنوز تأثیری بر درمان بالینی نداشته باشد.
به عبارت دیگر:
CBP ابزار بالینی برای تصمیمگیری درمانی است، در حالی که ECOFF ابزار اپیدمیولوژیک برای پایش ظهور مقاومتهای جدید به شمار میرود.