ژنهای مقاومت آنتیبیوتیکی در دام و محیط اطراف فراوان شده اند و عمدتاً از مقاومت ذاتی، جهش و انتقال ژن افقی ناشی میشوند. انتشار آنها از طریق کود، فاضلاب و آئروسل رخ میدهد و میتواند به میکروبیوتای انسانی منتقل شود. مصرف بیش از حد آنتیبیوتیکها سویههای چنددارویی ایجاد میکند، ساختار سلولی و پمپهای افلاکس باکتریها مقاومت را تقویت میکنند و مواجهه انسانی، عفونتهای مقاوم، اختلال میکروبیوتا و انتقال زئونوتیک را به همراه دارد. رویکرد سلامت واحد و جایگزینهای طبیعی مانند سینبیوتیک ها و ترکیبات گیاهی فشار انتخابی را کاهش میدهند.
ژن های مقاومت آنتی بیوتیکی حیوانات و خطرات پنهان آن برای سلامت جهانی
ژنهای مقاومت آنتیبیوتیکی به عنوان آلایندههای نوظهور محیطی در فارم ها و محیطهای اطراف آنها شایع هستند. ظهور این ژنها در محیطهای پرورش حیوانات عمدتاً ناشی از مقاومت ذاتی و جهشهای ژنتیکی است، در حالی که گسترش آنها عمدتاً توسط انتقال ژن افقی هدایت میشود. این ژنها از طریق مسیرهایی مانند کاربرد کود، تخلیه فاضلاب و انتشار آئروسل به محیط اطراف منتشر میشوند. آنها ممکن است توسط انسانها جذب شده و در میکروبیوتای روده تجمع یابند و در نتیجه بر سلامت انسان تأثیر بگذارند. ریزوستوم دام به عنوان مجموعه ژنهای مقاومت در میکروبیوم دام عمل میکند و شامل هزاران ژن مقاومت آنتیبیوتیکی است که بسیاری از آنها قابلیت انتقال به انسان را دارند. این ریزوستوم در گونههای مختلف دام مانند طیور، خوک و گاو متفاوت است و بیشترین ریسک انتقال، از مرغداریها ناشی میشود زیرا میکروبیوم مرغ حاوی ژنهای مقاوم بیشتری است که به راحتی به انسان منتقل میشوند. ژنهای مقاومت اغلب در پلاسمیدها قرار دارند که انتقال افقی را تسهیل میکنند و این فرآیند در محیطهای پرجمعیت فارم ها شتاب مییابد. عوامل محیطی مانند دما و رطوبت بر پایداری این ژنها در خاک و آب تأثیر میگذارند و باعث میشوند که آنها برای مدت طولانی در اکوسیستم باقی بمانند. مواجهه انسانی با این ژنها از طریق مصرف محصولات دامی یا تماس با محیط آلوده رخ میدهد و میتواند منجر به عفونتهای مقاوم شود که درمان آنها دشوار است.
نقش مصرف آنتیبیوتیک در دامداری در ایجاد مقاومت چنددارویی
مصرف آنتیبیوتیکها شامل اهداف درمانی، متافیلاکتیک، پروفیلاکتیک و افزایش رشد است. استفاده بیش از حد آنتیبیوتیکها، از جمله کاربرد پروفیلاکتیک و متافیلاکتیک و همچنین کاربرد برای افزایش رشد، فشارهای انتخابی را تشدید میکند و منجر به تکثیر سویههای باکتریایی مقاوم چنددارویی (MDR یا Multiple Drug Resistance) میشود. پاتوژنهایی مانند اشریشیا کلی، سالمونلا و استافیلوکوکوس اورئوس میتوانند از طریق تماس مستقیم، غذای آلوده و محیط به انسان منتقل شوند. مقاومت چنددارویی در باکتریهای پاتوژن به دلیل توانایی فوقالعاده آنها در سازگاری از طریق مکانیسمهای مقاومت ذاتی و اکتسابی افزایش مییابد. مقاومت ذاتی از جهشهای ژنتیکی ناشی میشود و باکتریها را قادر میسازد تا اهداف دارو را تغییر دهند، آنتیبیوتیکها را از طریق آنزیمهایی مانند بتالاکتامازها خنثی کنند یا جذب دارو را از طریق پروتئینهای غشایی تغییر یافته کاهش دهند. مقاومت اکتسابی عمدتاً توسط انتقال ژن افقی تسهیل میشود که شامل انتقال ژنهای مقاومت از طریق پلاسمیدها، اینتگرونها و ترانسپوزونها است. مصرف آنتیبیوتیکها در دامداری نه تنها برای درمان عفونتهای باکتریایی بلکه برای جلوگیری از بیماری در گلههای سالم نیز اعمال میشود و این کاربرد گسترده باعث انتخاب باکتریهای مقاوم میگردد. باکتریهای مقاوم در روده دام تجمع مییابند و از طریق مدفوع به محیط منتقل میشوند و چرخه مقاومت را ادامه میدهند. آنتیبیوتیکهای وسیعالطیف مانند تتراسایکلینها و پنیسیلینها بیشترین تأثیر را در ایجاد مقاومت دارند زیرا طیف گستردهای از باکتریها را هدف قرار میدهند و فشار انتخابی را افزایش میدهند. یکی از راهکارهای آینده نگرانه کاهش مصرف آنتی بیوتیک های شیمیایی استفاده از ترکیبات طبیعی مانند آنتی بیوتیک کاملا گیاهی آریوبیوتیک (ArioBiotic) است که دارای گواهی ثبت جهانی بوده و به عنوان اولین آنتی بیوتیک گیاهی دنیا شناخته شده است . همچنین علاوه بر اثر وسیع الطیف بر ضد باکتری ها، به واسطه ترکیبات موثر گیاهی موجود در آن دارای اثرات ضدالتهابی و آنتی اکسیدانی نیز می باشد.
برای اطلاعات بیشتر درمورد آنتی بیوتیک گیاهی آریوبیوتیک اینجا کلیک کنید.
ساختار سلول و مقاومت آنتیبیوتیکی
باکتریها از مکانیسمهای متنوعی برای مقاومت در برابر آنتیبیوتیکها استفاده میکنند که بسیاری از آنها با ساختار سلولی مرتبط هستند:
- باکتریهای گرم منفی دارای غشای خارجی محافظ هستند که جذب دارو را کاهش میدهد.
- تغییرات در ساختار یا تعداد پروتئینهای متصل به پنیسیلین منجر به مقاومت در برابر داروهای بتالاکتام میشود.
- پمپهای افلاکس که در غشای سلولی قرار دارند، مواد سمی را از سلول خارج میکنند و بسیاری از آنها ترکیبات متنوعی را حمل میکنند. کاهش تعداد پورینها در غشا نفوذپذیری را محدود میکند و داروهای هیدروفیل را تحت تأثیر قرار میدهد.
تغییرات در ترکیب یا ساختار هدف در باکتری مانع از تعامل آنتیبیوتیک با هدف میشود. این تغییرات اغلب در ژنهای کدکننده آنزیمهای سنتز دیواره سلولی رخ میدهند و ساختار پپتیدوگلیکان را تغییر میدهند. حفاظت هدف توسط پروتئینهای اضافی انجام میشود که آنتیبیوتیک را از هدف دور نگه میدارند و این مکانیسم در مقاومت به فلوروکینولونها رایج است.
- برخی باکتریها پروتئینهای جایگزین تولید میکنند که به جای پروتئینهای مهار شده توسط آنتیبیوتیک استفاده میشوند.
- دیواره سلولی متفاوت در باکتریهای مقاوم به وانکومایسین تولید میشود که از اتصال آنتیبیوتیک ممانعت میکند و نفوذپذیری غشا تغییر مییابد تا آنتیبیوتیکها نتوانند به هدف برسند.
- آنزیمهای تخریبکننده آنتیبیوتیک مانند آمینوگلیکوزید استیل ترانسفرازها در سیتوپلاسم سلول عمل میکنند و دارو را غیرفعال میسازند.
- تغییرات در ریبوزومها که هدف آنتیبیوتیکهای ماکرولید هستند، ساختار سلولی را تغییر میدهند و اتصال دارو را کاهش میدهند.
- بیوفیلمها که ساختارهای سلولی جمعی هستند، مقاومت را افزایش میدهند زیرا لایههای خارجی آنها مانع نفوذ دارو میشوند.
مسیرهای انتقال ژنهای مقاومت از دام به محیط و انسان
ژنهای مقاومت آنتیبیوتیکی از مزارع دام به محیط اطراف منتشر میشوند و مسیرهای انتقال شامل کاربرد کود، تخلیه فاضلاب و آئروسل است. انتقال ژن افقی بین باکتریهای مختلف در محیط رخ میدهد و پلاسمیدها نقش کلیدی در این فرآیند ایفا میکنند. فاضلاب مزارع حاوی باکتریهای مقاوم است که از طریق رودخانهها و کانالها به منابع آب انسانی میرسند. سیستمهای فیلتراسیون پیشرفته برای حذف این ژنها ضروری است و نظارت مداوم بر کیفیت آب کمک میکند تا ریسک کاهش یابد.
آئروسلهای تولید شده در مزارع از طریق هوا منتقل میشوند و میتوانند مسافتهای طولانی را طی کنند. کاربرد کود حیوانی در مزارع کشاورزی ژنها را به خاک وارد میکند و از طریق گیاهان به زنجیره غذایی میرسد. مواجهه انسانی از طریق نوشیدن آب آلوده یا مصرف سبزیجات رخ میدهد و عفونتهای مقاوم را ایجاد میکند. عوامل محیطی مانند pH و غلظت نمک بر بقای این ژنها در آب تأثیر میگذارند و پایداری آنها را افزایش میدهند.
عوارض آنتیبیوتیکهای قوی
استفاده بیش از حد آنتیبیوتیکهای قوی در دامداری منجر به ایجاد باکتریهای مقاوم میشود که درمان عفونتها را دشوار میکند. مصرف آنتیبیوتیکها عوارض جانبی ایجاد میکند و مقاومت در باکتریهایی مانند اشریشیا کلی و سالمونلا توسعه مییابد. باکتریهای مقاوم از طریق تماس مستقیم، غذای آلوده و محیط به انسان منتقل میشوند و عفونتهای مقاوم ایجاد میکنند. استفاده غیر درمانی فشار انتخابی تشدید میکند و سویههای مقاوم چنددارویی را تکثیر میکند. عفونتهای مقاوم درمان را پیچیده میکند و بار بهداشتی را افزایش میدهد. آنتیبیوتیکهای قوی مانند گلیکوپپتیدها و کارباپنمها عوارض شدیدی مانند اختلال در تعادل میکروبیوتا ایجاد میکنند و فرصت برای رشد باکتریهای فرصتطلب فراهم میآورند. مقاومت به این داروها منجر به عفونتهای طولانیمدت میشود و نیاز به درمانهای ترکیبی دارد که عوارض بیشتری به همراه دارند. انتقال زئونوتیک باعث شیوع عفونتهای مقاوم در جوامع انسانی میگردد و هزینههای درمانی را افزایش میدهد.
تأثیر بر میکروبیوتای انسانی و حیوانی
آنتیبیوتیکها میکروبیوتای روده را مختل میکنند و باکتریهای مقاوم در روده تجمع مییابند. این اختلال سلامت را تحت تأثیر قرار میدهد و عفونتهای طولانیمدت ایجاد میکند. کاهش تنوع میکروبی منجر به مشکلات گوارشی میشود و سیستم ایمنی را ضعیف میکند. باکتریهای مفید از بین میروند و جای خود را به پاتوژنهای مقاوم میدهند که التهاب ایجاد میکنند. در این موارد به منظور برقراری تعادل میکروفلور سودمند دستگاه گوارش و کاهش عوارض ناشی از مصرف آنتی بیوتیک ها می توان از سین بیوتیک MLC بهره برد که علاوه بر آن موجب تقویت سیستم ایمنی موضعی و عمومی شده و با افزایش سلامت و یکپارچگی دستگاه گوارش به بهبود رشد، وزن گیری و ضریب تبدیل حیوانات کمک می کند.
برای اطلاعات بیشتر درمورد مکمل سین بیوتیک MLC اینجا کلیک کنید
برای خرید مکمل سین بیوتیک MLC اینجا کلیک کنید
خطرات زئونوتیک و انتقال به انسان
پاتوژنهای مقاوم چنددارویی از دام به انسان منتقل میشوند و عفونتهای شدید ایجاد میکنند. تماس با حیوانات و مصرف محصولات آلوده ریسک را افزایش میدهد. این انتقال از طریق پوست، تنفس یا گوارش رخ میدهد و عفونتهای سیستمیک را به وجود میآورد. پاتوژنها در انسان تکثیر میشوند و مقاومت را به سایر باکتریها منتقل میکنند.
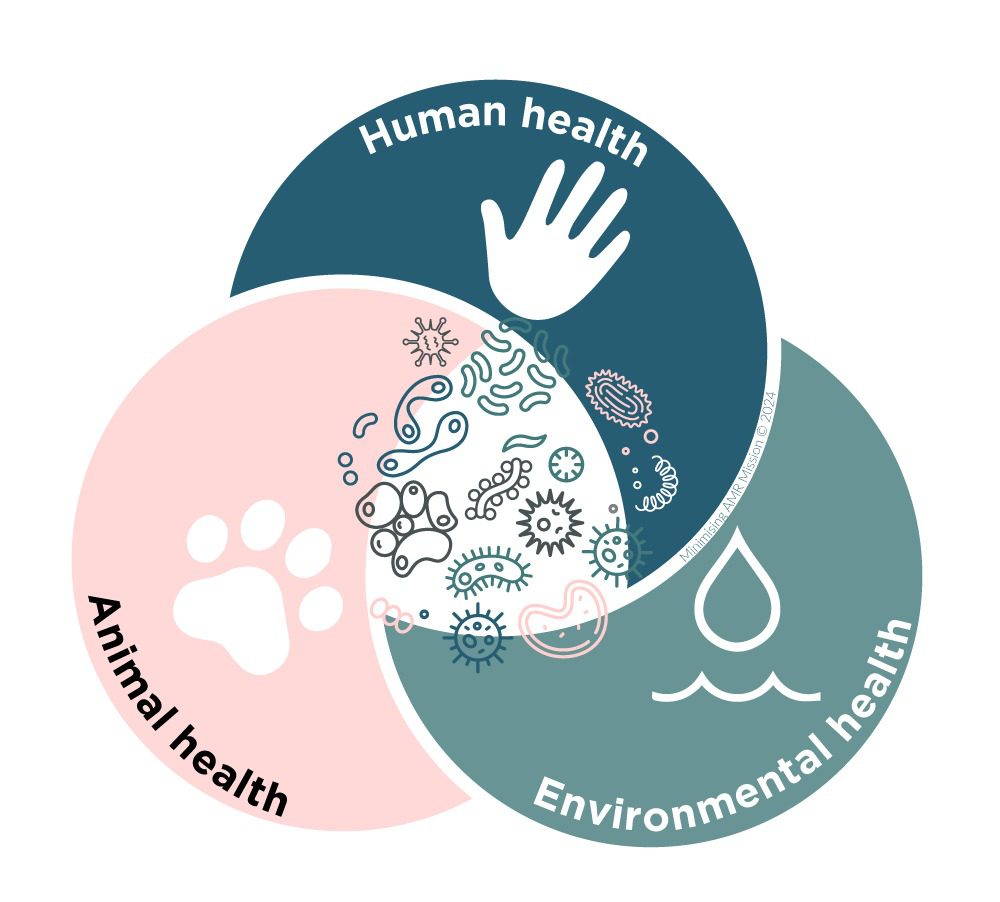
رویکرد سلامت واحد (One health) در مقابله با مقاومت آنتیبیوتیکی
مقابله با مقاومت آنتیبیوتیکی نیازمند رویکرد سلامت واحد است که ارتباط بین سلامت انسان، حیوان و محیط را تقویت میکند. کاهش ظهور ژنهای مقاومت در منابع، کنترل گسترش آنها و به حداقل رساندن مواجهه انسانی استراتژیهای کلیدی هستند. نظارت بر مصرف آنتیبیوتیک و شیوههای پایدار ضروری است تا سلامت عمومی حفظ شود. همکاری میانرشتهای و مدیریت آنتیبیوتیک بایستی تقویت شود تا تهدید مقاومت کاهش یابد. رویکرد سلامت واحد شامل نظارت یکپارچه بر میکروبیوم دام، محیط و انسان است و سیاستهای کاهش مصرف آنتیبیوتیک را ترویج میدهد. جایگزینهای آنتیبیوتیک مانند واکسنها و سین بیوتیکها و ترکیبات گیاهی استفاده میشوند تا فشار انتخابی کاهش یابد. آموزش پرورش دهندگان در مورد مدیریت صحیح آنتیبیوتیک ضروری است و سیستمهای تصفیه فاضلاب پیشرفته برای جلوگیری از انتقال ژنها باید مدیریت شوند.